Une encre est une préparation plus ou moins consistante, diversement colorée, utilisée pour écrire, dessiner ou imprimer. Ell est composée principalement d'un colorant qui lui confère sa couleur, d'un solvant, dans lequel le colorant ou le pigment est dispersé ou dilué, et d'un mordant qui permet de fixer l'encre sur le support.
Problématique: Peut-on créer une encre effaçable à partir de produits naturels?
Expérience
1. Composition du jus de chou rouge et de betterave
-
Le chou rouge
Le chou rouge est un indicateur coloré de pH, c'est-à-dire une espèce chimique qui change de couleur selon le pH de la solution aqueuse dans laquelle elle est dissoute.
Sa couleur vient de la cyanidine, qui appartient au groupe des anthocyanes, et se situe dans les protoplastes, des cellules sans paroi. C'est lors de la destruction de ses liaisons que le chou rouge change de couleur.
Formule topologique de la cyanidine
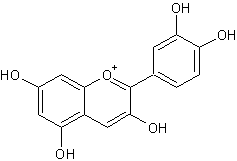
- La betterave rouge
La betterave rouge est l'une des trois sortes de betteraves existantes. C'est une plante de la famille des Amaranthaceae.
Tout comme le chou rouge, c'est un indicateur coloré de pH.
Sa couleur vient de la bétanine, contenue dans la racine de la betterave rouge.
Formule topologique de la bétanine
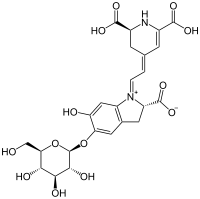
2. Protocole de fabrication de l'encre de jus de chou rouge et de betterave
- L'encre de jus de chou rouge
Tout d'abord, nous avons découpé une feuille de chou rouge à l'aide d'une paire de ciseaux.


Puis, nous avons mixé et écrasé les morceaux obtenus à l'aide d'un mortier.


Nous avons ensuite ajouté de l'eau distillée dans un cas et de l'éthanol dans un autre pour rendre plus liquide le jus de chou rouge obtenu. L'eau distillée et l'éthanol servent de solvant dans lequel est dilué le jus de chou rouge.


Après, nous avons utilisé la filtration pour ne garder que le jus de chou rouge et le solvant utilisé.
Cependant, cela s'est avéré plus difficile que nous ne le pensions. En effet, malgré le fait que nous ayons mixé puis écrasé une grande quantité de morceaux de chou rouge découpés, le jus de chou rouge a été obtenu difficilement et en très petite quantité comme nous pouvons le constater sur la 2ème et 3ème image.




Enfin, nous avons chauffé les deux préparations de jus de chou rouge, l'une étant composée de jus de chou rouge et d'eau distillée, l'autre de jus de chou rouge et d'éthanol, afin de ne garder que le jus de chou rouge.


- L'encre de jus de betterave
Contrairement au jus de chou rouge, le jus de bettrave a été obtenu très facilement. En effet, le jus était déjà présent dans le sachet de betteraves que nous nous sommes procurées. Malgré le fait qu'il soit très liquide, nous avons réalisé une filtration pour être sûres de n'avoir que du jus de betterave.

Voilà l'encre de betterave obtenue:

A partir de ces "encres organiques" obtenues, nous avons cherché un agent capable de les effacer. Ainsi, nous nous sommes interressées au dithionite de sodium et à l'eau oxygénée...
3. Réalisation de l'expérience
Nous avons versé dans 8 tubes à essais les mélanges suivants:
-jus de chou rouge + eau distillée (expérience témoin) => violet
-jus de chou rouge + eau ditillée + eau oxygénée = > marron clair
-jus de chou rouge + eau distillée + dithionite de sodium = > jaune clair
-jus de chou rouge + éthanol (expérience témoin) = > violet
-jus de chou rouge + éthanol + eau oxygénée = > marron clair
-jus de chou rouge + éthanol + dithionite de sodium = > jaune clair transparent
-jus de betterave (expérience témoin) = > rouge
-jus de betterave + dithionite du sodium = > rouge clair
-jus de betterave + eau oxygénée = > orange clair transparent
Nous avons ainsi remarqué que seul les solutions jus de chou rouge + dithionite de sodium et jus de chou rouge + éthanol + dithionite de sodium ont été "effaçées". Elles sont devenues jaune clair, presques tranparentes.

De plus, deux semaines plus tard, nous avons remarqué que les solutions ont changé de couleur:
-jus de chou rouge + eau distillée (expérience témoin) => violet
-jus de chou rouge + eau distillée + eau oxygénée => jaune
-jus de chou rouge + eau distillée +dithionite de sodium => transparent trouble
-jus de chou rouge + éthanol (expérience témoin) => violet
-jus de chou rouge + éthanol + eau oxygénée => jaune clair
-jus de chou rouge + éthanol +dithionite de sodium => trouble
-jus de betterave + eau distillée (expérience témoin) => marron jaune
-jus de betterave + eau distillée + eau oxygénée => jaune clair transparents
-jus de betterave + eau distillée + dithionite de sodium => jaune clair transparent
Nous savons que le chou rouge (agent colorant: cyanidine) et la betterave (agent colorant: bétanine) sont des marqueurs colorés de l'acidité.
Donc, le dioxyde de carbone présent dans l'air peut être à l'origine de ce changement de couleur en se solubilisant dans les solutions. L'environnement (température, air...) peut également avoir participer à ce changement.
Résultats de l'expérience
Nous pouvons en déduire que seul le dithionite de sodium a une action d'effaceur sur l'encre de chou rouge.
Cependant, l'effacement de l'encre de chou rouge est-il dû au pH de la solution, dont l'acidité aurait brisé des liaisons conjuguées de la molécule de cyanidine, ou à un phénomène de dilution?
Pour cela, nous avons comparer le pH des différentes solutions...
-
Mesures de pH

pH jus de chou rouge: 3,8 => violet
pH jus de chou rouge diluée : 3,7 => rose violacé
pH jus de chou rouge + dithionite de sodium: 4,3 = > jaune trouble
pH jus de chou rouge + dithionite de sodium après 2 semaines: 4,5 => trouble
pH jus de betterave: 4,8 = > rouge
pH jus de betterave diluée : 4,7 => rouge clair
pH jus de betterave + dithionite de sodium: 5 => rouge clair/orangé
pH jus de betterave + dithionite de sodium après deux semaines: 4,6 => incolore et transparent
Les résultats suggèrent un phénomène de dilution puisque l'écart de pH entre du jus et du jus dilué est négligeable (0,1).
Cependant, nous ne nous sommes pas contentées que de ce résultat. En effet, à côté, nous avons procédé à une recherche de
vérification:
https://lucid-state.org/community/images/5/51/Choux_rouge.JPG
Ce tableau nous indique clairement que notre résultat est faux car le changement de pH d'une solution à une autre est insuffisant
pour constater un changement de couleur. Par exemple, le pH de jus de chou rouge + dithionite de sodium ne peut pas être 4,3
avec une couleur jaune car pour avoir cette couleur, le pH doit être de 11 ou 12. Nous pensons donc nous être trompées dans nos mesures du pH.
De plus, voici le tableau de la couleur du jus de betterave rouge en fonction du pH du solvant dans lequel il est dissous:
| 0 |
12< pH <14 | |
| Couleur d'un jus de betterave | Rouge | Jaune |
Source: BATAILLE, Xavier, LE RILLE, Alain, BEAUVINEAU, Erwan, MARIE, Jean-Xavier. Physique-Chimie 1ère. BELIN, 2011. Chap. 5, Substances organiques colorées, p.93-131.
Le jus de betterave apparaissant rouge clair/orangé en présence de dithionite de sodium, nous pouvons suppposer, grâce au tableau ci-dessus, que le pH du jus de betterave serait plus logiquement près de 11, ce qui concorderait avec nos hypothèses précédentes.
Par ailleurs, durant une séance de TP en chimie sur " Paramètres influençant la couleur d'une substance", nous avons appris
que le chou rouge, tout comme la betterave, est un indicateur coloré qui change de couleur en fonction du pH.
Nous pouvons en déduire que sous l'action du dithionite de sodium, rendant le jus de chou rouge basique (c'est-à-dire avec un pH supérieur à 7), des liaisons conjuguées de la cyanidine ont été détruites, comme nous pouvons le remarquer ci-dessous. Cela a provoqué son changement de couleur: le jus de chou rouge passe du violet au jaune clair.

Formule topologique de la cyanidine lorsque le jus de chou rouge apparaît violet
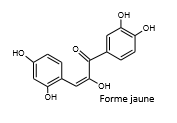
Formule topologique de la cyanidine lorsque que le jus de chou rouge apparaît jaune
